Иммунотерапия при раке молочной железы
Содержание
Иммунотерапия рака молочной железы

Онкологическая клиника в Москве ¦ ИММУНОТЕРАПИЯ В ОНКОЛОГИИ ¦ Иммунотерапия рака молочной железы
Проблема рака молочной железы
Рак молочной железы относится к самым распространенным видам рака у женщин. Хотя в странах Западной Европы намечается тенденция к снижению заболеваемости и смертности от данного вида опухоли, в России и Восточной Европе эти показатели демонстрируют устойчиво высокие цифры.
Ежегодный рост заболеваемости раком молочной железы во всем мире составляет около 3%. В Москве каждый год выявляют порядка 5500 первичных опухолей груди.
Рак молочной железы очень часто обнаруживают в поздней стадии, что делает лечение таких пациенток затруднительным, а иногда – малоперспективным.
В настоящее время главным средством борьбы с опухолью молочной железы служит хирургический метод, но даже радикальная мастэктомия не всегда решает проблему. Клетки опухоли имеют тенденцию диссеминировать лимфогенным путем и давать метастазы, а также прорастать в соседние анатомические области.Химиотерапия и облучение не самые оптимальные методы, поскольку не обладают избирательностью и поражают здоровые клетки организма, особенно эпителиоциты и клетки кроветворной системы, что дает множество неблагоприятных побочных эффектов в виде анемии, кровоточивости, выпадения волос, инфекционных осложнений и т.д. По этой причине медицинский и научный мир неустанно ищет новые способы помощи женщинам для более избирательной и безопасной борьбы со злокачественным новообразованием.
Иммунотерапия, как направление в борьбе с онкологическими заболеваниями, появилась не так давно, но уже получила определенную «популярность» в медицинских кругах. Как самостоятельный метод ее редко применяют, обычно она сопровождает традиционные способы лечения.
Очень хорошим свойством иммунотерапии является ее высокая избирательность и нацеленность исключительно на раковые клетки, а здоровые клетки, как правило, не затрагиваются.
Этот метод способен оказывать не только лечебное, но и профилактическое воздействие, снижая вероятность заболеть определенными видами рака в будущем.
Иммунотерапия в Европейской клинике
В Европейской клинике хирургии и онкологии применяют самые передовые разработки во всех возможных направлениях медицины для помощи онкологическим больным. Изначально эта организация создавалась по типу онкологической клиники.
Здесь есть собственный хосписный центр, отделение управления болью, онкоцентр, реанимация.
Руководство и врачебный состав клиники постоянно контактирует со своими коллегами из Московского Онкологического Центра для решения сомнительных ситуаций и сложных случаев.
Персонал Европейской клиники представлен опытными специалистами с блестящими результатами в профессиональной деятельности, что вкупе с отличными технологическими возможностями учреждения дает высокий процент благоприятных исходов и минимум осложнений при лечении онкологических больных.Иммунотерапевтическое направление давно и успешно используется в комплексной терапии пациентов, что существенно улучшает исход большинства патологических состояний, связанных со злокачественными новообразованиями.
Вклад иммунотерапии в лечение рака молочной железы
В лечении рака иммунотерапевтическое направление предлагает множество препаратов с различными механизмами действия, которые так или иначе воздействуют на реакции иммунитета. Иммунотерапию в изолированном виде редко применяют.
Иногда ее назначают неоперабельным пациентам в целях продления жизни и борьбы с мелкими метастазами, которые не удается выявить диагностическими методами.
В других ситуациях ее применяют после облучения или курса химиотерапии, что позволяет снизить дозу этих токсичных препаратов, но в то же время усилить общую эффективность лечения.
Иммунотерапия предлагает много приемов, основными из которых являются: вакцинирование против определенных видов опухолей или онкогенных вирусов; использование моноклональных антител (в том числе конъюгированных с радио- или химической меткой) для уничтожения измененных клеток; применение активированных лимфоцитов; введение цитокинов, интерферонов, противоопухолевых белков, ингибиторов клеточного цикла; назначение иммуностимуляторов.
Методы воздействия на иммунитет при опухоли условно делятся на активные и пассивные. К активным относят вакцинирование и использование активированных лимфоцитов, к пассивным – назначение цитокинов, иммуномодуляторов, моноклональных антител.
Чаще всего при раке молочной железы используют моноклональные антитела, которые выпускают в виде препаратов: герцептина, кадсила, трастузумаба и др.
При разработке этих антител были использованы эпитопы раковых клеток молочной железы, которые не наблюдаются в нормальных тканях.
Иногда антитела конъюгируют с химиопрепаратами или радиоактивной меткой и после того, как произойдет реакция антиген-антитело, опухолевая клетка уничтожается.
Моноклональные антитела дают меньше побочных эффектов, чем химиотерапия или облучение. Тем не менее, у них тоже есть свои отрицательные стороны.
Это обусловлено возможной перекрестной реакцией антиген-антитело, когда антитела реагируют с эпитопами здоровых клеток, которые имеют сходное строение с раковыми антигенами. Это связано с антигенной вариабельностью и никогда не бывает 100%-й гарантии отсутствия осложнений.
Моноклональные антитела иногда взаимодействуют с клетками сердечно-сосудистой, дыхательной систем и эмбриональными тканями.Основными соматическими осложнениями могут быть признаки сердечной недостаточности, которая характеризуется снижением толерантности к физической нагрузке, одышкой, появлением отеков. Может повышаться артериальное давление. Иногда бывают случаи расстройства стула.
Доказано тератогенное действие, поэтому принимать препараты на основе моноклональных антител во время беременности категорически запрещено. Если после родов возникает такая необходимость, то следует выждать 7 месяцев.
Ничего не известно насчет влияния таких лекарств на грудное молоко, но врачи рекомендуют воздерживаться от их приема в период лактации.
Активировать иммунную систему онкобольного
После окончания основного лечения, которое включает курсы радио- и химиотерапии, у пациентки, как правило, сильно страдает иммунная система, что провоцирует ряд серьезных осложнений инфекционного характера. В таких ситуациях часто назначают иммуностимулирующие препараты, которые могут усиливать как антибактериальный, так и антивирусный иммунитет.
Обычно предписывают растительные медикаменты (эхинацею, элеутерококк), препараты тимуса, витамины, биогенные стимуляторы, компоненты микробной стенки и др. Это позволяет активировать иммунную систему не только в отношении микробов, но и усилить противоопухолевый иммунитет.
В настоящее время получили экспериментальные доказательства эффективного применения активированных Т-лимфоцитов против опухоли груди, в том числе в составе адъювантной терапии с тамоксифеном и противоопухолевым белком апоптином. Кроме того, была доказана эффективность фактора некроза опухоли и других белков, но их широкое внедрение в общеклиническую практику только предстоит.
Все больше появляется научных статей и диссертаций с доказательством успешности различных иммунотерапевтических приемов и это позволяет надеяться, что в ближайшем будущем произойдет снижение смертности и инвалидизации от рака молочной железы.
+7(925)191-50-55 — европейские протоколы лечения в Москве
ЗАПРОС в КЛИНИКУ
Источник: http://www.rusmedserv.com/oncoclinic/Immunotherapyoncology/Mammarycancer/
17 препаратов иммунотерапии, используемых для лечения разных видов рака

Величайшим достижением современной онкологии в лечении рака за рубежом является разработка и внедрение в клиническую практику различных препаратов, способствующих созданию противоракового иммунитета.
Эти лекарства имеют биологическое происхождение, они не токсичны, не вызывают побочных эффектов и угнетения различных функций организма больного, как химиопрепараты.
Научной базой для создания такого метода лечения являются открытия в области иммунологии, в частности, у онкологических больных.
Препараты иммунотерапии в современной онкологии
Установлено, что при злокачественных опухолях в организме пациентов всегда имеет место снижение его защитных свойств, то есть иммунитета.
Далее, учеными, исследующими иммунологию рака в крупнейших онкологических центрах мира, было обнаружено, что потенциальные раковые клетки (незрелые клетки различных тканей) ежедневно образуются в больших количествах у каждого человека. Теоретически это создает такую ситуацию, что каждый человек ежедневно рискует заболеть 6-8 видами рака.
Но у большинства людей этого не случается по той причине, что постоянно срабатывает иммунная система и обезвреживает эти аномальные клетки, воспринимая их как чужеродные, и рак развивается именно тогда, когда защитная функция организма недостаточна.
Это и легло в основу идеи создания препаратов, которые могли бы естественным образом воздействовать на злокачественные клетки – как профилактически, не давая возможности развиться опухоли, так и с целью воздействия на уже имеющуюся раковую опухоль. Сегодня арсенал таких препаратов довольно широк, и он постоянно пополняется, а применение этих лекарств в клинической практике доказывает их эффективность при лечении различных форм рака у взрослых и у детей.Более подробную информацию о возможности пройти иммунотерапию рака можно получить на нашем сайте, заполнив форму контакта. В течение суток предоставляется бесплатная консультация ведущего онколога, вся необходимая информация и всесторонняя организационная помощь в прохождении лечения в выбранной клинике.
Закажите бесплатную консультацию
Интересные исторические факты иммунотерапии в онкологии
Препараты иммунотерапии – это новое, перспективное и еще недостаточно изученное направление в онкологии, но корнями своими оно уходит к концу 19-го века. Американский хирург Вильям Коли в 1891 г.
обнаружил уникальную закономерность у онкологических больных, переболевших стрептококковой инфекцией (рожистым воспалением, скарлатиной). Спустя время после этих инфекций он отметил обратное развитие, уменьшение опухолей, в частности, саркомы.
Это побудило его к созданию первой противораковой вакцины на базе ослабленных возбудителей инфекционных заболеваний. При введении в организм они не вызывали развития инфекции, а лишь стимулировали иммунную систему, и образовавшиеся антитела воздействовали на опухоль.
Ученый получил серию хороших результатов в лечении рака, но его метод был подвергнут критике как противоестественный и опасный.
Лишь спустя много лет, в 60-е годы прошлого века, с развитием иммунологии и открытием различных факторов иммунитета (интерлейкина, интерферона, факторов роста и т.д.) положило начало системному созданию и применению иммунопрепаратов в онкологии. А с развитием генетики в 1991 г.
был выявлен первый онкоген, кодирующий злокачественный рост. В настоящее время таких мутантных генов уже выявлено множество разновидностей и принадлежность их к развитию того или иного вида опухоли.
И сами иммунные препараты уже создаются не методом иммунизации человека или лабораторных животных, а методом генной инженерии (перекодирования генов).
Механизм воздействия и основные группы препаратов иммунотерапии
Все современные препараты иммунотерапии в онкологии по механизму действия разделяются на 3 основных группы:
- Создающие активный специфический иммунитет, это противораковые вакцины, содержащие антиген конкретной опухоли и побуждающие организм вырабатывать специфические антитела против нее.
- Неспецифические иммунопрепараты или иммуномодуляторы, повышающие в целом защитные свойства организма, выработку защитных иммунных тел.
- Моноклональные антитела – принципиально новое направление в иммунотерапии рака, это – создание в лабораторных условиях специфических иммунных белковых тел из одной единственной клетки, то есть это специфическая, точечная или клеточная иммунотерапия рака.
Противораковые вакцины для иммунотерапии
Противоопухолевых вакцин создано множество разновидностей, они делятся по способу получения и действия на следующие подгруппы:
- клеточные вакцины, в состав которых входят целые опухолевые клетки (аутологичные – данного пациента или аллогенные – другого пациента с подобным видом рака);
- антигенные вакцины, действующим фактором которых является лишь антиген, извлеченный из опухолевых клеток.
В клеточных вакцинах содержатся раковые клетки, ослабленные и лишенные способности к развитию и делению, поэтому они не могут «заразить» пациента раком, а лишь вызывают выработку на них иммунных тел.
В состав антигенных вакцин входят не целые раковые клетки, а лишь их различные компоненты: белки, генетический материал (ДНК, РНК).
Для их введения используются специальные вирусы-проводники, которые не вызывают заболевания, а лишь способствуют транспортировке антигенов к иммунной системе.
Примерами наиболее используемых в практике вакцин являются Oncophage (Витеспен), Onyvax, Cancer-Vax, NY-ESO-1, ALVAC-CEA, VG-1000, TRICOM, Prostvac и другие.Одни из них являются моновалентными, предназначенными для одного вида рака, другие – поливалентными, которые можно применять для лечения нескольких видов рака.
Одни вакцины уже широко применяются в клинической практике, целый ряд новых вакцин проходят клинические испытания, постоянно ведется научный поиск и разработка более эффективных вакцин.
Неспецифические иммунопрепараты в онкологии, адьюванты
Эти препараты оказывают общее стимулирующее действие на иммунную систему, и таким образом усиливают в том числе и противораковый иммунитет. Они обычно применяются как адьюванты – дополнение к другим препаратам для усиления выработки специфического противоопухолевого иммунитета.
Наибольшее применение в онкологии получили следующие препараты:
- иммуномодуляторы – Талидомид, Ревлимид, Ромалист, а также бацилла Кальметта-Герена (BCG), то есть то, что нам известно, как БЦЖ – иммунизация ослабленной микобактерией туберкулеза;
- цитокины – белковые молекулы, влияющие на активность иммунных клеток и их деление: Интерлейкин-2, Интерферон-альфа, Колониестимулирующий фактор, Сарграмостин.
Моноклональные антитела в иммунотерапии
Открытие и создание моноклональных антител совершило революцию в иммунотерапии рака. Они представляют собой иммунные белки, вырабатываемые одной клеткой (клоном), потому обладают специфичным направленным действием именно на подобные клетки.
По механизму действия выделяют 2 группы моноклональных антител:
- неконъюгированные – оказывающие самостоятельное воздействие на раковую клетку и «помечающие» опухоль для иммунной системы;
- конъюгированные, или препараты целевого (таргетного) действия, несущие на себе к раковым клеткам молекулы химиопрепарата или же радиоактивные изотопы;
Наиболее широко применяются именно неконъюгированные моноклональные антитела, кроме «указательной» функции они сами воздействуют на клетки рака – угнетают факторы роста, активность ферментов, блокируют ангиогенез (образование новых сосудов в растущей опухоли).
Примерами подобных препаратов являются Алемтузумаб для лечения лейкемии за границей, Ритуксимаб для лечения лимфомы, Эрбитукс для лечения рака толстой кишки, Герцептин для лечения рака молочной железы за рубежом, Рамуцирумаб для лечения рака желудка и другие препараты.
Конъюгированные моноклональные антитела – новое направление в комбинированном лечении рака, объединяющее в себе сразу 2 метода: радио- и иммунотерапию и химио- и иммунотерапию. Например, Ибритумомаб (Зевалин), применяемый для лечения лимфомы, Трастузумаб длялечения рака молочной железы.
В настоящее время в США и Европе ведутся работы по созданию поливалентных и гуманизированных моноклональных антител, а также конъюгированных с микроэлементом селеном, повышающим эффективность лечения.
Узнайте точную стоимость лечения
Препараты иммунотерапии для разных видов рака
Препараты иммунотерапии показаны на всех стадиях рака и практически при раке любой локализации. На ранних стадиях рака они сыграют большую роль в предупреждении метастазирования опухоли в лимфоузлы и органы, а также существенно снизят вероятность ее рецидива после лечения, укрепят иммунную систему.
На поздних, метастатических стадиях рака они способствуют замедлению развития опухоли и ее распространения, а коньюгированные препараты отыщут вторичные раковые очаги в любом участке организма и проведут таргетное воздействие химиопрепаратом или радиоактивными частицами, непосредственно на клеточном уровне, не повреждая при этом здоровых тканей.
Припараты иммунотерапии при раке легкого
В комплексе лечения рака легких применяются:
- Бевацизумаб (Авастин) – ингибитор ангиогенеза, лишающий опухоль притока крови и приводящий к задержке ее развития, применяется в сочетании с химиопрепаратами, содержащими платину;
- Бавитуксимаб – воздействует на внешнюю белковую защиту раковых клеток и делает их заметными для иммунной системы организма;
- Патритумаб – оказывает блокирующее воздействие на белковый механизм деления раковых клеток, обычно применяется в сочетании с препаратом Эрлотиниб.
Припараты иммунотерапии при раке простаты
Для лечения рака простаты наиболее применяемы следующие препараты:
- Вакцина GVAX – клеточная вакцина, оказывающая блокирующее влияние на рост раковых клеток;
- Вакцина PROSTVAC – изготовлена на основе опухолевого антигена PSA и содержит вирусный «проводник» (из ослабленного вируса оспы кур);
- Вакцина Прованж (Provenge) – терапевтическая клеточная вакцина, изготавливаемая для каждого пациента индивидуально в специальной лаборатории;
- Вакцина ProstAtak – конъюгированная вакцина; содержащая молекулы цитостатика Валацикловира и вирусный проводник для доставки препарата непосредственно раковым клеткам;
- Ипилимумаб (Yervoy) – моноклональное антитело, активизрующее цитотоксическое действие Т-лимфоцитов и повышающее иммунный ответ за счет обнаружения раковых клеток.
Припараты иммунотерапии при раке молочной железы
При раке молочной железы, в основном, применяются вакцины и моноклональные антитела:
- Герцептин – содержит моноклональные антитела, блокирущие белок HER-2 в раковых клетках, тем самым препятствующие их росту и развитию;
- Вакцина Neuvenge – эффективна при наиболее агрессивном HER-2 позитивном раке груди;
- Вакцина РЕСАН (создана в Беларуси) – включает более 40 разновидностей антигенов опухоли, создает клеточный противораковый иммунитет с формированием «памяти» иммунитета, что значительно снижает число рецидивов рака;
- Тайкерб (Лапатиниб) – оказывает действие, подобное Герцептину, но имеет более широкий спектр эффективности, и применяется в сочетании с Кселодой, когда Герцептин оказывается малоэффективным.
Припараты иммунотерапии при раке желудка
Для лечения рака желудка в комплексе с химиотерапией применяются следующие иммунные препараты:
- Иматиниб (Тайверб) – моноклональное антитело, блокирующее рецепторы роста раковой клетки;
- Бортезомиб (Велкейд) – ингибитор белкового обмена в раковых клетках, повреждает структуру ДНК, повышает чувствительность опухоли к химиотерапевтическим препаратам;
- Эверолимус – препарат применяется как ингибитор иммунитета при пересадке органов, но обнаружено его сильное угнетающее действие на раковые клетки путем блокирования фермента АТФ.
Припараты иммунотерапии меланомы
Одна из самых злокачественных опухолей – меланома, устойчивая ко многим химиопрепаратам, оказалась более «податливой» к воздействию иммунотерапии:
- Ниволумаб – является моноклональным антителом таргетного действия, блокирует рост опухолевых клеток;
- Пембролизумаб (Кейтруда) – моноклональное антитело, блокирует защитный белок PD-1 меланомных клеток, делая их заметными для иммунной системы.
Большой опыт применения подобных препаратов накоплен в лечении рака в Израиле, где эффективность терапии меланомы является самой вкоысой.
Проконсультируйтесь с врачом Online
Где можно пройти лечение рака иммунопрепаратами
Иммунотерапия рака за границей – новый и пока еще дорогостоящий метод лечения рака, тем более, что большинство современных препаратов выпускаются западными фармацевтическими кампаниями. Поэтому, если ваш выбор падает на отечественной онкологии, то такое лечение можно пройти в столицах России, Украины, Казахстана, Беларуси.
Если же вы можете позволить себе лечение за границей, то во всех онкологических центрах развитых стран оно доступно на самом высоком уровне, а цены на лечение рака за рубежом более демократичными будут в клиниках Израиля. Более подробно узнайте обо всем через контактную форму на сайте.
Источник: https://www.oncomedic.org/%D0%BF%D1%80%D0%B5%D0%BF%D0%B0%D1%80%D0%B0%D1%82%D1%8B-%D0%B8%D0%BC%D0%BC%D1%83%D0%BD%D0%BE%D1%82%D0%B5%D1%80%D0%B0%D0%BF%D0%B8%D0%B8
История лечения рака молочной железы виротерапией — Лечение рака

Метастазы в печени, в случае рака молочной железы, обычно ассоциируются с плохим прогнозом. Мы рассматриваем случай, когда пациенту с раком груди и метастазами в печени удалось существенно продлить жизнь. После хирургической операции пациент отказалась от дальнейшего лечения традиционными методами.
Вместо этого в «Иммунологическом и Онкологическом Центре» (Кёльн, Германия), к ней было применено лечение локальной гипертермией, вирусом болезни Ньюкасла и вакциной дендритных клеток. Было отмечено непрерывное высокое качество жизни и пациент прожил более 66 месяцев после первоначального диагноза.
Под воздействием лечения не было рецидива или дальнейшего развития метастазов. Также, лечение вызвало долгосрочный ответ противоопухолевой Т-клеточной памяти. Возможно это объясняет благоприятное течение болезни.
Так как данное сочетание терапий не ограничивается в применении определенным видом опухоли, дальнейшее изучение весьма оправдано.
В Германии, на сегодняшний день, рак молочной железы является наиболее часто встречающейся злокачественной опухолью у женщин, регистрируется около 70 000 случаев в год.
Рак молочной железы с метастазами в печени на данный момент считается неизлечимым и имеет плохой прогноз. Средний период жизни — 6 месяцев без лечения и 14-22 месяца с химиотерапией.
Сейчас принято прибегать к более традиционному лечению, включающему в себя хирургическое вмешательство, гормоно-, химио- и радио-терапию (лучевую терапию), а также антитела.
К сожалению, обычное лечение влечет за собой серьезные побочные эффекты, которые могут ухудшить качество жизни. Для сравнения, направленная иммунотерапия не вызывает серьезных побочных эффектов, так как затрагивает только злокачественные клетки и не влияет на здоровую ткань.
Дендритные клетки (ДК), введенные посредством противоопухолевой вакцины, это важная часть иммунотерапевтической стратегии. Они служат для стимуляции противоопухолевого ответа посредством Т-клеток, эффективного в случае различных видов злокачественных опухолей, включая рак молочной железы.
Доктор Куриглиано (Curigliano G — разрабатывает эффективную вакцину против рака молочной железы) считает вакцинацию ДК «клинической реальностью» в случае лечения рака молочной железы. Доктор Гелао заявляет, что иммунотерапия это «общепризнанный ключевой элемент в лечении рака, в том числе рака груди».
Он предоставил комплексное исследование доклинических испытаний и более 20 клинических испытаний с применение вакцинации ДК против рака молочной железы.Другой многообещающий подход заключается в использовании онколитических вирусов нацеленных непосредственно на клетки опухоли.
Вирус болезни Ньюкасла (ВБН) — это птичий РНК парамиксовирус, чрезвычайно безопасный для больных онкологическими заболеваниями.
Свойства, делающие ВБН подходящим для борьбы с человеческим раком, это репликация исключительно в клетках опухоли, противоопухолевая цитотоксичность и иммуностимуляция.
Гипертермия применяется для лечения широкого круга твердых опухолей. Она оказывает воздействие на иммунную систему, активируя натуральные опухолевые киллеры, также как и ДК. Радиочастотная гипертермия также способствует выделению белков теплового шока (БТШ) и аптозу злокачественных клеток.
Данное исследование представляет собой отчет о комбинированном лечении с применением гипертермии, онколитической виротерапии и вакцинации ДК. Ранее, мы публиковали отчет о случае долгосрочной ремиссии рака предстательной железы с обширными метастазами в костях, в котором применялся схожий метод лечения.
История болезни
В октябре 2009 года, 70 летняя пациентка поступила в «Иммунологический и Онкологический Центр» (ИОЦ; Кёльн, Германия) с инвазивным проточным раком молочной железы и первичными метастазами в печени.
Пациентка уже подвергалась сегментарной резекции левой груди и удалению подмышечных лимфатических узлов в октябре 2009 года, вскоре после первоначальной диагностики. После хирургической операции стадия была pT1c pN0 (0/10) M1 L0 V0 R0 G2. Статус гормональных рецепторов был ER80%, PR 5%, HER2/Neu 50%.
Рентген грудной клетки и сцинтиграфия не показали наличие метастазов. Ультразвук выявил как минимум шесть метастазов в печени, позже подтвержденных биопсией. Гистологически, метастазы без сомнения были вызваны раком молочной железы.
Согласно принятым в Германии нормам, пациенту советовали начать прием Летрозола и в случае прогрессии метастазов в печени — начать химиотерапию. Но пациент, однако, отказался от традиционного лечения в целом и предпочел направленную иммунотерапию.
Иммунотерапия
В период с декабря 2009 по апрель 2010 года, пациент проходил лечение в ИОЦ, при помощи радиочастотной гипертермии (РГТ) печени совместно с системной онколитической ВБН виротерапией примерно дважды в месяц. В дополнение, пациент получил пять вакцинаций с ДК, импульсированных лизатом из ВБН-инфецированных раковых клеток груди.
С октября 2010 года по декабрь 2012 года, пациента лечили при помощи РГТ печени и виротерапией примерно раз в месяц для чтобы поддержать иммунный ответ. В мае 2012 года, ПЭТ выявила прогресс метастазов в размере. Также, тест методом иммуноферментных пятен (ELISPOT) выявил сокращение количества Т-клеток противоопухолевой памяти.
В связи с этим, вакцинации были возобновлены. Пациент получил еще три вакцины с ВБН-активированными поляризированными клетками ДК1 в мае 2012, декабре 2012 и феврале 2013 года. С ноября 2013 по июнь 2014, пациент ежемесячно получал лечение РГТ и ВБН.
В апреле и мае 2014, а также с октября 2014 года и далее, лечение в виде РГТ, ВБН и умеренной гипертермии всего тела проводилось каждые 4-6 недель.Гипертермия проводилась оборудованием Oncothermia EHY-2000 на радиочастоте 13 МГц. В итоге, пациент прошел 52 процедуры гипертермии печени. Длительность каждой сессии была 50 минут, начиная с 50 Ватт и достигая максимально 80 Ватт за сессию, также пациент получил 10 в седьмой степени единиц ВБН (онколитический штамм MTH-68) внутривенно для достижение нагретой опухолевой ткани.
ДК были дифференцированы из аутологичных моноцитов крови при помощи гранулоцитарно-макрофагального колониестимулирующего фактора и IL-4. Для первых пяти вакцин, незрелые ДК были испульсированы лизатом из клеток рака груди MDA-MB-453.
Лизат содержал равные доли уже инфицированных ВБН клеток и клеток предварительно обработанных гипертермией. После созревания ДК, импульсированные клетки были введены внутрикожно. Для последних трёх вакцинаций, незрелые ДК были активированы при помощи ВБН для получения поляризированных клеток ДК1.
Умеренная гипертермия всего тела увеличила температуру тела до 38.5-40.0°C.
Итог и следствие
В ноябре 2010 года, ПЭТ выявила семь метастазов в печени. Другое сканирование в мае 2012 года указало на прогрессию этих метастазов в размере, но не выявило новых отдаленных метастазов. В июле 2014 года ПЭТ/КТ свидетельствовали об отсутствии прогрессии по сравнению с ПЭТ в мае 2012. Локальный рецидив и возникновение отдаленных метастазов были также исключены.
Для оценки успеха вакцинации и уверенности в отсутствии необходимости дальнейших вакцинаций, велось наблюдение за Т-клеточным ответом пациента. Был проведен тест с изолированными Т-клетками и лизат-импульсированными ДК из периферической крови, краткосрочный анализ позволил оценить Т-клеточный ответ противоопухолевой памяти.
Т-клетки выделяющие гамма-интерферон в процессе краткосрочного контакта (40 ч.) с лизат-испульсированными аутологичными ДК были посчитаны. Результаты проиллюстрированы на рисунке 1. Они начинаются с первого теста перед вакцинацией и заканчиваются последним тестом осуществленным в январе 2014.
Ответ Т-клеточной памяти возрос после вакцинаций, но сократился в 2012 году. После возобновления ДК вакцинации, был восстановлен глубокий отклик Т-клеточной памяти. Эти данные совпадают с клиническим курсом: слабый Т-клеточный ответ в мае 2012 года соответствует прогрессу метастазов в печени согласно ПЭТ.
После возобновления сильного ответа Т-клеточной памяти, метастазы в печени оставались стабильны согласно ПЭТ/КТ в июне 2014 года.
Лечение пациент перенес хорошо. Отмечено непрерывное высокое качество жизни. Пациентка сама ведет домашнее хозяйство. Не было ни одной госпитализации после первичной операции. На данный момент пациентка жива уже более 66 месяцев после первичной диагностики.
На публикация всех вышеуказанных данных и изображений было получено письменное согласие пациента.
Заключение
Комбинация взятых вместе различных иммунотерапевтических стратегий спровоцировало долгосрочный ответ Т-клеточной памяти и привело к благоприятному течению курса у данного конкретного пациента.
На сегодняшний день, сотни пациентов с различными видами рака прошли курс лечения в ИОЦ с применением схожих стратегий лечения. Это привело к положительным результатам примерно у 80% вакцинированных.
Учитывая множественные положительные клинические результаты и незначительные побочные эффекты, данный подход заслуживает дальнейшего исследования. В будущем, идентификация прогнозируемых факторов отзывчивости у пациента поможет повысить ответную реакцию на лечение.
Исследование частных случаев, таких как случай описанный выше, может выявить важные инновации и пополнить наши знания в области медицины. Частный случай, по утверждению Фармацевтического Закона Германии, имеет важное значение для пациентов и медицинского прогресса.- Рак груда — наиболее часто встречающаяся злокачественная опухоль у женщин.
- Метастазы в печени значительно ухудшают прогноз.
- Традиционные методы лечения, такие как хирургия, гормоно-, химио- и радио-терапия или антитела часто приводят к серьезным побочным эффектам.
- Направленная иммунотерапия затрагивает только клетки опухоли и потому на несет серьезных побочных эффектов.
- Вакцинация дендритных клеток (ДК), использование онколитических вирусов и гипертермия — важные компоненты иммунотерапевтической стратегии.
История болезни
- 70-летний пациент страдающий от инвазивного проточного рака молочной железы с первичными метастазами в печени, подвергалась сегментарной резекции груди.
- После операции стадия была pT1c pN0 (0/10) M1 L0 V0 R0 G2, статус гормональных рецепторов был ER 80%, PR 5%, HER2/Neu 50%.
- Пациент отказался от типичного лечения вопреки медицинским советам и выбрал иммунотерапию.
Иммунотерапия
- С декабря 2009 по апрель 2010 года, пациент проходил лечение радиочастотной гипертермией (РГТ) печени совместно с системной виротерапией онколитическим вирусом болезни Ньюкасла (ВБН) и получил 5 вакцинаций лизат-импульсированных ДК.
- Впоследствии, ежемесячные сессии РГТ и ВБН проводились для поддержания иммунного ответа.
- Пациент получил еще три вакцинации в период с мая 2012 по февраль 2013 год.
- С ноября 2013 по июнь 2014 года, пациент ежемесячно подвергался лечению РГТ и ВБН.
- В апреле и мае 2013, а также начиная с октября 2014, лечение проводилось каждые 4-6 недель, при помощи РГТ, ВБН и умеренной гипертермии всего тела.
Итог и следствие
- Т-клеточный ответ на вакцины отслеживался методом ELISPOT.
- После первых пяти вакцин, задокументирован хороший ответ Т-клеточной памяти.
- Контроль в 2012 году выявил сокращение числа реагирующих Т-клеток, что совпало с прогрессией метастазов в печени.
- После следующих трёх вакцинаций, ответ Т-клеточной памяти был успешно восстановлен.
- Последний контроль в январе 2014 года выявил долгосрочный ответ Т-клеточной памяти.
- ПЭТ/КТ показали отсутствие прогрессии метастазов в печени в июне 2014. Локальный рецидив и возникновение отдаленных метастазов были также исключены.
- Лечение пациент перенес хорошо. Отмечено непрерывное высокое качество жизни. Пациентка сама ведет домашнее хозяйство. Не было ни одной госпитализации после первичной операции. На данный момент пациентка жива уже более 66 месяцев после первичной диагностики.
Заключение
- Иммунотерапия комбинирующая в себе РГТ, ВБН и вакцинации ДК привела к долгосрочной противоопухолевой Т-клеточной памяти и сопровождалась благоприятным течением курса со стабилизацией болезни, у данного конкретного пациента.
- Комбинация РГТ, ВБН и вакцинации ДК предстает перед нами как многообещающий инструмент для лечения.
- Идентификация прогнозируемых факторов отзывчивости у пациента будет иметь важное значение.
Авторы: Volker Schirrmacher, Wilfried Stücker, Maria Lulei, Akos-Sigmund Bihari и Tobias Sprenger
Рак молочной железы, как и другие виды рака, при благоприятных условиях можно эффективно лечить виротерапией. Но для более детального прогноза — требуются документы из Вашего лечебного заведения. Только изучив результаты анализов, врач-онколог может назначить или наоборот не рекомендовать виротерапию.
Подать документы
[addtoany]
Источник: http://viroterapiya.com/istoriya-lecheniya-raka-molochnoi-zhelezi-viroterapiey/
Может ли иммунотерапия использоваться для метастатического рака молочной железы?

Иммунотерапия — новая область лечения рака. В последние годы этот вид лечения оказался успешным в повышении выживаемости у людей с определенными видами рака. Это включает метастатический рак предстательной железы и метастатический рак легких.
Исследователи теперь изучают иммунотерапию рака молочной железы. Некоторое время они не соглашались с ролью иммунной системы при раке молочной железы. Более поздние исследования показывают, что иммунная система играет важную роль.
Продолжайте читать, чтобы узнать больше о том, как работает иммунотерапия, и о типах иммунотерапии, которые сейчас изучаются для лечения рака молочной железы.
РекламаРеклама
Иммунотерапия
Как действует иммунотерапия?
Иммунотерапия — это тип лечения, которое использует собственную иммунную систему организма для борьбы с раковыми клетками. Иммунная система работает, атакуя вещества в организме, которые она не распознает.
Это включает вирусы, бактерии и раковые клетки. Раковые клетки представляют собой большую проблему, потому что они могут не отличаться от нормальных клеток иммунной системой.
Иммунотерапия помогает иммунной системе лучше бороться с раковыми клетками.
Различные виды иммунотерапии работают по-разному. Некоторые типы работают, повышая вашу иммунную систему, чтобы помочь ей работать лучше. Другие дают вашей иммунной системе больше инструментов, таких как антитела, для атаки на конкретные раковые клетки.
Существует четыре основных типа иммунотерапии, которые исследователи изучают для лечения метастатического рака молочной железы:
- вакцины против рака
- ингибиторы контрольной точки
- приемная терапия Т-клеток
- моноклональные антитела
Раковые вакцины
Раковые вакцины
Эти вакцины работают, стимулируя иммунитет, который атакует и убивает раковые клетки. Первая противораковая вакцина, одобренная Управлением по контролю за продуктами и лекарствами США (FDA), была вакциной для людей с метастатическим раком предстательной железы. Показано, что эта вакцина увеличивает общую выживаемость у людей с метастатическим раком предстательной железы.
В настоящее время многие стратегии вакцинации изучаются у людей с раком молочной железы. Некоторые исследователи считают, что вакцины против рака молочной железы могут работать лучше всего в сочетании с другими видами терапии.
Люди, которые не получили много лечения, также могут воспользоваться вакцинами. Вакцины могут занять месяцы, чтобы вызвать иммунный ответ, поэтому они могут не подходить для раковых заболеваний поздней стадии при использовании в одиночку. Они могут по-прежнему играть важную роль при использовании с другими видами терапии. Исследования в этой области продолжаются.
РекламаРекламаРеклама
Ингибиторы контрольных точек
Ингибиторы контрольных точек
У иммунной системы есть определенные контрольные точки, которые помогают удержать ее от нападения на нормальные клетки в организме.Эти контрольно-пропускные пункты также могут ослабить атаку иммунной системы на раковые клетки. Контроллеры контрольных точек — это препараты, которые препятствуют работе определенных контрольных точек. Это делает иммунный ответ сильнее.
FDA уже одобрило несколько препаратов этого класса для использования при меланоме и метастатическом раке легкого. Клинические испытания ингибиторов контрольных точек, используемые отдельно и в сочетании с другими видами терапии, также ведутся для людей с метастатическим или тройным отрицательным раком молочной железы.
Adoptive T-cell therapy
Adoptive T-cell therapy
Т-клетка — это тип лейкоцитов, который играет важную роль в иммунном ответе. Adoptive терапия Т-клеток включает удаление ваших Т-клеток, их модификацию, чтобы улучшить их активность, а затем вернуть их вам через инъекцию. В настоящее время проводится несколько ранних исследований для тестирования этого подхода у женщин с метастатическим или тройным отрицательным раком молочной железы.
РекламаРеклама
Моноклональные антитела
Моноклональные антитела
Моноклональные антитела могут быть изготовлены в лаборатории. Они атакуют очень специфические части раковой клетки. Моноклональные антитела могут быть «голыми», что означает, что они работают в одиночку. Они также могут быть «сопряженными», что означает, что они соединены с радиоактивной частицей или химиотерапевтическим препаратом.
Лечение метастатического рака молочной железыМетастатический рак молочной железы отличается от одного человека к другому в зависимости от того, где рак распространился. Лечение может варьироваться довольно часто и должно быть адаптировано к вашим потребностям. Лечение обычно фокусируется на предотвращении рецидивов, устранении или уменьшении боли и сохранении вашего качества жизни.
Уже имеются моноклональные антитела, доступные для лечения рака молочной железы. Трастузумаб (Герцептин), обнаженное моноклональное антитело, нацеливается на HER2-положительный белок.
Этот белок содержится в некоторых клетках рака молочной железы. Ado-trastuzumab emtansine (Kadcyla), конъюгированное моноклональное антитело, прикрепляется к химиотерапевтическому препарату.
Он также нацелен на HER2-положительный белок.
В настоящее время изучается ряд других моноклональных антител в качестве лечения прогрессирующего рака молочной железы.
Реклама
Побочные эффекты
Каковы побочные эффекты иммунотерапии?
Иммунотерапия обычно считается менее побочной, чем другие виды лечения рака. Однако некоторые люди могут по-прежнему испытывать побочные эффекты.
Возможные побочные эффекты могут включать:
- лихорадка
- озноб
- усталость
- головная боль
- тошнота
- рвота
- диарея
- слабость
- низкое кровяное давление
- высыпания
Более серьезные последствия могут иметь место в легких, печени, почках и других органах. Вакцины обычно вызывают только незначительные побочные эффекты. Вы также можете испытывать реакции на месте инъекции, такие как зуд или покраснение. Они со временем уменьшаются.
РекламаРеклама
Перспективы
Перспективы
В настоящее время иммунотерапия в основном изучается для лечения метастатического рака молочной железы, но она также выглядит перспективной для использования на других стадиях рака молочной железы.
Многие клинические испытания продолжаются, и ожидается, что скоро появятся новые методы лечения.Их успех будет зависеть от поиска правильного подхода к конкретному типу и стадии рака молочной железы. Также вполне вероятно, что терапия будет наиболее полезна, когда они сочетаются с другими видами лечения.
Поговорите со своим врачом о новых вариантах лечения, которые могут быть доступны. Узнайте о новых методах лечения. Вы также можете принять участие в клиническом исследовании. Многие из этих исследований предназначены для людей с метастатическим раком молочной железы и уже получали или в настоящее время получают другие виды лечения рака.
Источник: https://ru.medic-life.com/can-immunotherapy-be-used-for-metastatic-breast-cancer-18813
Иммунотерапия рака молочной железы (груди) | Европейская клиника
Иммунотерапия — метод лечения онкологических заболеваний, который использует ресурсы иммунной системы для уничтожения раковых клеток.
До относительно недавнего времени рак молочной железы считался «иммунологически безмолвным». В настоящее время проведено немало исследований, которые показали, что некоторые виды иммунотерапии могут повысить эффективность лечения рака молочной железы, они имеют некоторые преимущества по сравнению с классической химиотерапией.
На данный момент иммунотерапия рака молочной железы — одно из наиболее активно развивающихся направлений в онкологии. Существует острая потребность в новых эффективных методах лечения, так как рак груди по-прежнему остается актуальной проблемой:
- Это один из наиболее часто диагностируемых у женщин типов рака. Он составляет 12% от всех онкологических заболеваний.
- Рак молочной железы находится на втором месте среди причин женской смертности от злокачественных опухолей.
- В 2012 году насчитывалось 1,7 миллиона новых диагнозов и полмиллиона смертей.
- Несмотря на то, что смертность от рака груди снижается, заболеваемость продолжает расти.
Виды иммунотерапии при раке груди
Выделяют две большие группы иммунотерапии при онкологических заболеваниях:
- Активная иммунотерапия задействует собственные ресурсы иммунной системы. Ученые пытаются найти антигены раковых клеток, которые могли бы стать мишенью для иммунной атаки, затем разрабатывают методы, которые помогли бы «натравить» иммунитет на эти вещества. К этой группе можно отнести противораковые вакцины, T-клеточную терапию.
- Пассивная иммунотерапия предусматривает введение в организм факторов иммунной защиты, которые помогают уничтожать раковые клетки. К пассивным методам иммунотерапии можно отнести лечение цитокинами, ингибиторами контрольных точек.
Существуют разные виды иммунотерапии при онкологических заболеваниях:
- противораковые вакцины;
- иммуномодуляторы;
- ингибиторы контрольных точек;
- онколитические вирусы;
- T-клеточная терапия;
- адъювантная иммунотерапия;
- моноклональные антитела;
- цитокины.
Но далеко не все это реально применяется в клинической практике при раке молочной железы. Многие методы пока проходят клинические испытания.
Виды препаратов
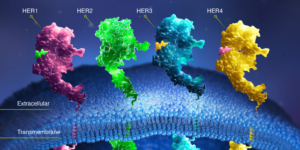
Злокачественные опухоли молочной железы могут обладать разными молекулярно-генетическими свойствами, и это определяет их восприимчивость к тем или иным методам лечения. На поверхности некоторых клеток увеличено количество белка-рецептора HER2. Его активация заставляет раковые клетки размножаться. Рак груди является HER2-позитивным примерно у каждой пятой пациентки.
В настоящее время американским Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) одобрены для клинического применения три иммунопрепарата (их же относят к таргетным препаратам) из группы моноклональных антител: трастузумаб (герцептин), пертузумаб (перьета), трастузумаб эмтанзин (кадсила). Другие виды иммунотерапии пока проходят клинические испытания.
В каких случаях применяется иммунотерапия при раке молочной железы?
Моноклональные антитела применяют в случаях, когда рак является HER2-позитивным. Проверить это можно с помощью молекулярно-генетического анализа опухолевой ткани.
Иммунотерапия имеет некоторые преимущества перед химиотерапией:
- Она действует более прицельно, не повреждает здоровые клетки, и поэтому вызывает меньше побочных эффектов.
- Благодаря тому, что иммунопрепараты более безопасны, их можно вводить в течение длительного времени, применять в комбинациях с другими препаратами, не боясь усиления токсичности.
- Иммунная система может использовать в качестве мишеней разные антигены злокачественных опухолей, поэтому во время лечения у пациентов реже развивается резистентность.
Побочные эффекты
Моноклональные антитела при раке груди могут вызывать некоторые побочные эффекты. В большинстве случаев они мягкие, но иногда могут быть серьезными.
У некоторых женщин развивается застойная сердечная недостаточность. В большинстве случаев (но не всегда) она сохраняется в течение короткого времени и проходит после завершения лечения.
Риски усиливаются, если ингибиторы контрольных точек применяют вместе с химиопрепаратами, особенно с доксорубицином и эпирубицином.
Нарушения со стороны сердца проявляются в виде одышки, отеков на ногах, постоянной сильной усталости.Пертузумаб может вызывать диарею.
Во время беременности моноклональные антитела опасны для плода, способны привести к его гибели. Поэтому, если есть вероятность, что пациентка беременна, врач не станет назначать данный вид иммунотерапии.
Получить заочную консультацию врача
Иммунопрепараты, которые проходят клинические испытания для лечения рака молочной железы
Моноклональные антитела. В настоящее время проводятся клинические испытания еще одного препарата, нацеленного на белок HER2 — маркетуксимаба, а также препаратов, которые смогут атаковать и блокировать другие «мишени»:
- Блокаторы VEGF (вещества, которое выделяют раковые клетки, чтобы стимулировать рост новых сосудов): бевацизумаб (авастин), рамицирумаб (цирамза).
- Блокаторы Wnt (молекулярного сигнального пути, который способствует росту опухоли): вантиктумаб (OMP-18R5).
- Блокаторы HER3 (белка, который помогает опухолевым клеткам приобрести устойчивость к лечению): препарат LJM716.
- Блокаторы клеточных белков, которые помогают опухолям метастазировать: препараты CDX-011 и IMMU-132.
Противораковые вакцины действуют по аналогии с вакцинами против инфекций. Они «обучают» иммунную систему атаковать те или иные антигены раковых клеток. В настоящее время проходят клинические испытания нескольких разных вакцин.
Ингибиторы контрольных точек. Иммунная система использует сложные молекулярные механизмы, чтобы сдерживать себя от атаки на здоровые клетки. Этими механизмами могут воспользоваться для «маскировки» раковые клетки. Существуют препараты, которые блокируют контрольные точки — вещества, сдерживающие иммунитет.
T-клеточная терапия. Суть метода состоит в том, что у пациента берут T-лимфоциты и в лабораторных условиях «обучают» их распознавать раковые клетки, обрабатывая некоторыми веществами или при помощи генной инженерии. Затем иммунные клетки возвращают в организм пациента, и они начинают атаковать опухоль. Сейчас проходят испытания разных методов T-клеточной терапии.
Онколитический вирус. Представляет собой генетически модифицированный вирус, который атакует и разрушает раковые клетки.
Адъюванты. Представляют собой химические вещества (чаще всего лиганды), которые связываются с рецепторами на поверхности клеток и усиливают или ослабляют иммунный ответ. Могут применяться отдельно или в сочетании с другими иммунопрепаратами.
Цитокины. Это небольшие информационные молекулы, которые могут стимулировать иммунную систему. В настоящее время при раке молочной железы проходят клинические испытания два препарата из этой группы: интерлейкин-2 и интерлейкин-7.
Стоимость иммунотерапии в Европейской клинике
Стоимость курса иммунотерапии — от 150 тыс. р.
Для подробного расчета получите консультацию врача.
Рассчитать стоимость курса
В Европейской клинике доступны наиболее современные химиопрепараты, иммунопрепараты, таргетные препараты для лечения рака груди и других онкологических заболеваний, одобренные на территории России.
Мы знаем, как помочь, если рак прогрессирует, если не помогает химиотерапия, которую вам назначили в другой клинике. Мы можем помочь пациентам, которые желают принять участие в клинических испытаниях новых препаратов.
Свяжитесь с нами.
Записьна консультациюкруглосуточно
Источник: https://www.euroonco.ru/departments/himioterapiya/immunoterapiya-raka-molochnoj-zhelezy-grudi